سوانت آرنیوس و نظریه تفکیک الکترولیتی: نگاهی به یکی از ستونهای علم شیمی
مقدمه
درک ما از رفتار محلولها و ترکیبات یونی مدیون نظریهای است که در قرن نوزدهم توسط شیمیدانی جوان از سوئد به جهان معرفی شد. سوانت آرنیوس (Svante Arrhenius) نه تنها با نظریه خود درباره تفکیک الکترولیتی جایگاه ویژهای در تاریخ شیمی بهدست آورد، بلکه بنیانگذار یکی از مهمترین تعاریف اولیه اسید و باز شد.
زندگینامه کوتاه سوانت آرنیوس
سوانت آگوست آرنیوس در سال 1859 در سوئد به دنیا آمد. او در دانشگاه اوپسالا تحصیل کرد و سپس با ارائه رسالهای انقلابی درباره رسانایی الکترولیتها در سال 1884، توجه جامعه علمی را جلب کرد. این رساله بعدها پایهگذار نظریه الکترولیتی او شد.
در سال 1903، آرنیوس بهخاطر تحقیقاتش در زمینه هدایت الکتریکی محلولها و نظریه تفکیک یونی، جایزه نوبل شیمی را دریافت کرد. او از نخستین دانشمندانی بود که درباره نقش دیاکسید کربن در گرمایش زمین هشدار داد.
نظریه تفکیک الکترولیتی آرنیوس
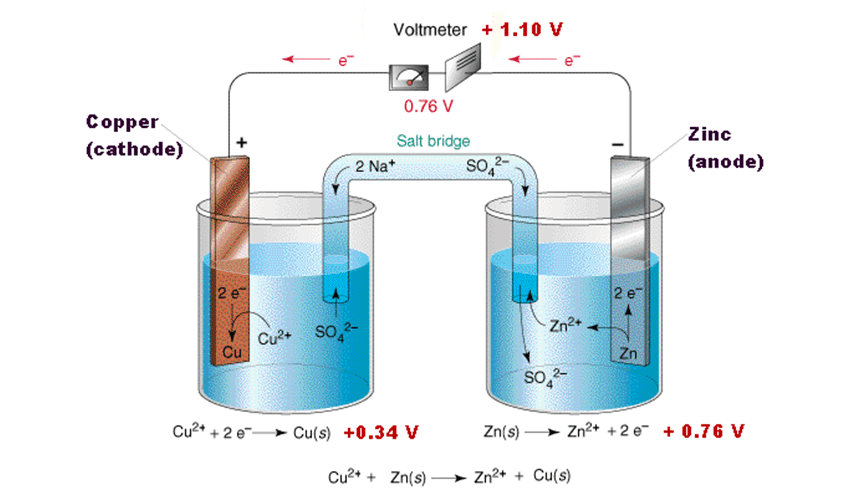
آرنیوس در نظریه خود بیان کرد که مواد الکترولیتی (مانند نمکها، اسیدها و بازها) در هنگام حل شدن در آب به یونهایی تجزیه میشوند. برای مثال:
–NaCl → Na⁺ + Cl
بر اساس این نظریه:
الکترولیت قوی: تقریباً به طور کامل به یون تجزیه میشود.
الکترولیت ضعیف: فقط بخشی از آن به یون تبدیل میشود.
این نظریه راه را برای درک واکنشهای شیمیایی در محلولهای آبی هموار کرد و نقطه شروعی برای نظریههای پیشرفتهتر اسید-باز شد.
تعریف اسید و باز از دیدگاه آرنیوس
آرنیوس اسید و باز را اینگونه تعریف کرد:
اسید: مادهای که در آب یون هیدروژن (⁺H) آزاد میکند.
مثال:
–HCl → H⁺ + Cl
باز: مادهای که در آب یون هیدروکسید (⁻OH) آزاد میکند.
مثال:
–NaOH → Na⁺ + OH
مزایای این تعریف:
ساده و قابل فهم
پایهگذار درک یونی واکنشها در محلول آبی
محدودیتها:
فقط به واکنشهای آبی محدود است
نمیتواند برخی اسیدها یا بازهایی را که در آب یون هیدروژن یا هیدروکسید تولید نمیکنند توجیه کند (مثل آمونیاک)
تأثیر آرنیوس بر شیمی مدرن
ایجاد زمینه برای نظریههای بعدی مثل نظریه برونستد-لوری و لوییس
پایهگذاری شیمی فیزیک و درک نوین از رسانایی الکترولیتی
پیشبینی اثر گلخانهای که یکی از دیدگاههای پیشگامانه در علم اقلیم است
مقایسه با نظریههای بعدی اسید و باز
| ویژگی | نظریه آرنیوس | نظریه برونستد-لوری | نظریه لوییس |
|---|---|---|---|
| مبنا | تولید H⁺ / OH⁻ | انتقال پروتون | انتقال جفت الکترون |
| محیط محدود | فقط آبی | گستردهتر | بسیار گسترده (حتی در گازها) |
| سادگی | بسیار ساده | متوسط | پیچیدهتر |
نتیجهگیری
سوانت آرنیوس با نظریه تفکیک الکترولیتی و تعریف سادهای از اسید و باز، درک ما از شیمی محلولها را متحول کرد. اگرچه نظریه او بعدها توسط نظریههای دقیقتری تکمیل شد، اما همچنان یکی از پایههای آموزش شیمی در جهان باقی مانده است. شناخت نظریه آرنیوس، درک بنیادینی از رفتار یونی مواد در آب و واکنشهای شیمیایی را به ما میدهد.